У Китаї вперше здійснили пересадку легені генетично модифікованої свині людині — пацієнту з діагностованою смертю мозку, який прожив із трансплантатом дев’ять днів. Процедуру провела команда з Першої афілійованої лікарні медичного університету Ґуанчжоу. Хоча орган зазнав поступового відторгнення, цей експеримент став важливою віхою у розвитку ксенотрансплантації. Про це повідомляє медіа про науку, технології та здоров’я КРВ.медіа з посиланням на текст дослідження, опублікований у журналі Nature Medicine.
Як проходив експеримент із пересадки легені свині людині
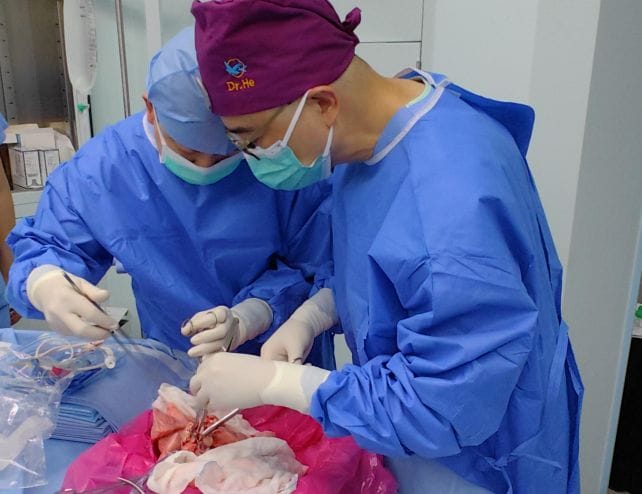
У серпні 2025 року хірурги з Першої афілійованої лікарні медичного університету Ґуанчжоу вперше у світі пересадили легеню генетично модифікованої свині пацієнтові з діагностованою смертю мозку. Донором став представник породи бама — мініатюрна свиня, яку часто використовують у біомедичних дослідженнях.
Цей поросюк мав шість генетичних змін, внесених за допомогою технології CRISPR. Цей метод дозволяє точно «редагувати» ДНК організмів — тобто видаляти або замінювати певні гени, зокрема ті, що викликають відторгнення органів. У цьому випадку редагування були спрямовані на зменшення імунної реакції людського тіла.
39-річного чоловіка, якому трансплантували орган, було офіційно визнано таким, що має смерть мозку після інсульту. Його родина надала письмову згоду на участь у науковому експерименті.
Під час операції легеню свині під’єднали до дихальних шляхів, судин та артерій пацієнта. Донорська тварина, як правило, не виживає після вилучення такого життєво важливого органа — про її подальшу долю в статті не повідомляється.
У перші години після втручання орган працював стабільно. Ознак гіперакцентованого відторгнення — гострої імунної реакції, яка зазвичай виникає одразу — не зафіксували. Але вже за 24 години в легені виник набряк, спричинений відновленням кровотоку в новому середовищі.
Чому саме органи свині?
Значна частина пацієнтів, які потребують пересадки органів, не отримують їх вчасно через гострий дефіцит донорів. Це змушує медиків і науковців шукати альтернативи, зокрема у сфері ксенотрансплантації — пересадки органів від тварин до людини.
Свині вважаються найбільш придатними до такої ролі: їхні органи схожі за розміром і функцією на людські, а генетичні модифікації допомагають адаптувати ці органи до людської імунної системи.
Однак трансплантація легень — найскладніше завдання. Легені постійно контактують із зовнішнім середовищем через повітря, тому мають особливо активні захисні механізми. Це робить їх надзвичайно чутливими до чужорідних тканин.
У цьому випадку легеня функціонувала протягом дев’яти днів — і хоча в підсумку експеримент завершився відторгненням, дослідники вважають його успішним кроком уперед.
Що виявили лікарі: імунна відповідь і дисфункція трансплантата
На третій та шостий день після операції лікарі зафіксували активну реакцію антитіл, яка почала пошкоджувати тканини легені. Результатом стало те, що в пацієнта розвинулась первинна дисфункція трансплантата — тяжке ураження пересадженого органа, що зазвичай виникає протягом перших 72 годин після трансплантації. Це одна з головних причин смертності після пересадки легень.
Попри пошкодження, на дев’ятий день у легені почали проявлятися ознаки часткового відновлення функцій. Проте на цьому етапі дослідники припинили підтримку життєдіяльності, адже мета експерименту — спостереження, а не тривале збереження органа.
У своїй науковій статті дослідники зазначили:
«Ранній розвиток набряку легені підкреслює важливість запобігання первинній дисфункції трансплантата у майбутніх випадках ксенотрансплантації легень. Надалі потрібно вдосконалювати імуносупресивні режими, генетичні модифікації, методи збереження органів і дослідження довготривалого функціонування трансплантата».
Майбутнє ксенотрансплантації: потенціал і бар’єри
Результати дослідження підтверджують, що ідея використання тваринних органів у медицині має наукове підґрунтя, однак реалізація її на практиці потребує подолання низки бар’єрів.
Серед них — ризики імунного відторгнення, необхідність постійного прийому імуносупресивних препаратів, етичні питання щодо використання тварин і складність організації спеціалізованих лабораторій для вирощування генетично змінених донорів.
Експеримент у Китаї підтвердив, що при належній підготовці можна уникнути найнебезпечнішої форми відторгнення — гіперакцентованої реакції. Це дає надію на подальше вдосконалення технології та поступове наближення ксенотрансплантації до клінічної практики.
Раніше ми також писали про першу операцію з повторної трансплантації серця в Україні